(香港文匯報記者 詹漢基)阿茲海默症(俗稱腦退化)是悄然無聲的大腦侵蝕者,患者表面上仍能獨自買餸煮飯,但該病其實已不斷蠶食大腦細胞,令其慢慢萎縮。初期患者或許出現健忘、反覆提問、情緒改變等情況,或會被誤以為是「正常老化」而沒有正視問題。事實上,當患者有一天在路上漫無目的地徘徊、無法辨認親友,那已經進入了病情無法逆轉的階段—而這個轉變很有可能在三五年內發生。
為盡早辨識早期阿茲海默症患者,香港的科研人員孜孜不倦地尋找全新的檢測方式,包括追蹤葡萄糖在大腦遊走的足跡,從而了解腦淋巴系統的運作情況;有團隊透過人工智能系統,捕捉大腦少至0.01ml的萎縮變化,從而判斷患上阿茲海默症的風險;有專家研發出創新的血液檢測技術,「全方位」捕捉大腦細微變化,未來甚至有望以一滴血就可「見微知著」,開拓了阿茲海默症檢測的新方向。
只要讀懂人體血液所蘊含的資訊,有助人類揭開疾病的神秘面紗。血液檢測已經廣泛運用在心血管疾病、糖尿病等,但原來人類也能藉血液了解大腦運作,未來甚至只靠一滴血就能診斷出是否患有阿茲海默症。由國際知名神經生物學家、香港科技大學副校長(研究及發展)葉玉如所領導的團隊,成功利用中國人群數據開發出簡單有效的血液檢測方法,辨別阿茲海默症患者的準確度高達96%,技術甚至能藉由大腦蛋白水平的變化,分辨病情的發展階段,為大規模篩查、分期診斷提供極大的應用前景。有關結果近日被國際權威科學期刊《Alzheimer's & Dementia: The Journal of the Alzheimer's Association》刊載,並引起學術界的熱烈討論。
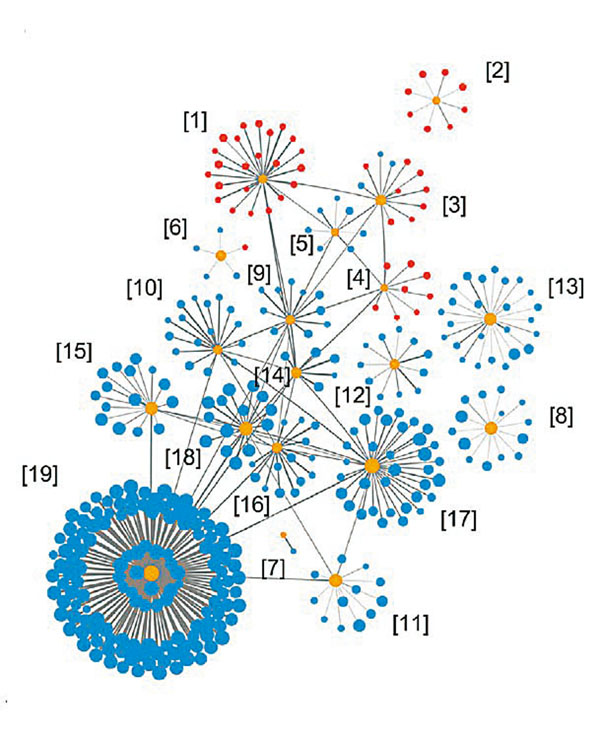
該研究論文的第一作者、科大生命科學部博士生江源冰表示,「身體各個器官組織發生病變時,會分泌特定蛋白,導致血液裏某種蛋白濃度發生變化;通過檢測相關蛋白,可以反過來得知是否有病。」阿茲海默症患者大腦的神經元死亡,會出現免疫反應、發炎等狀況,同樣會分泌特定蛋白,「例如NELL1實際上是神經元表達,更多反映患者大腦的神經活性狀態;比如KLK4等,是在免疫細胞裏面表達,反映患者的免疫系統狀態。」
團隊成員之一、科大生命科學部研究副教授傅潔瑜表示,團隊利用近年出現的超靈敏高通量鄰近延伸分析技術 (PEA),從約700名香港患者的血漿樣本中,檢測了約1,200種蛋白質的水平變化。團隊將429種與阿茲海默症相關的血漿蛋白,識別出19種具有該症患病特徵的血漿蛋白生物標誌物組群,「即每一個cluster(簇)中變化最大的作為代表,我們做了數學上的計算,以這19個蛋白代表那400多個蛋白。」
根據標誌物,研究人員設計了一套評分系統,按照血液中的蛋白比例「打分」,以判斷是否確診。系統的準確率不僅高達96%,而且只需從病人的靜脈抽取少量血液,配合特定試劑產生反應,兩到三天即可獲得結果,更能辨別屬於早期、中期、還是晚期。
有望將診斷時期提前10年
江源冰解釋,有些蛋白來自神經系統,有些則是來自免疫系統,「系統檢測的19種蛋白來自不同的系統及細胞,可以準確告訴患者是哪一個地方出現病變。」而且系統能捕捉大腦蛋白的細微變化,有望將診斷時期提前5年到10年。
大腦中的β澱粉樣蛋白(Aβ)斑塊及 Tau蛋白為阿茲海默症的反映,國際上不少團隊試圖在血液中透過找出單一蛋白實現血液檢測。江源冰表示,「單憑Aβ蛋白不足以斷症,因人體血液中特定的酶會導致Aβ斑塊自然分解,因此不夠穩定」,加上部分蛋白是在患病中後期才會出現,檢測單一蛋白難以篩查出早期患者。
江源冰表示,「我們需要找到新的蛋白、生物標誌物來進行診斷。我們系統同時檢測19種蛋白,這樣可以取得最大的準確性。」傅潔瑜補充指,比起觀察單一蛋白的數量,系統期望能反映早期病理變化,因此希望以多蛋白的數據呈現biological process(生物過程)。
是次主要研究中國人群組,江源冰指出,不同人種的蛋白水平可能會有變化,「若要把技術運用在西方人群,還要進行優化,這也是我們正在做的工作;我們正和世界不同地方的研究機構合作,希望收集更多血液樣本優化模型。」傅潔瑜則表示,希望將模型改良,「將19種蛋白慢慢減少的同時,能保持大致的準確度。」
中大研AI磁力共振助醫生斷症
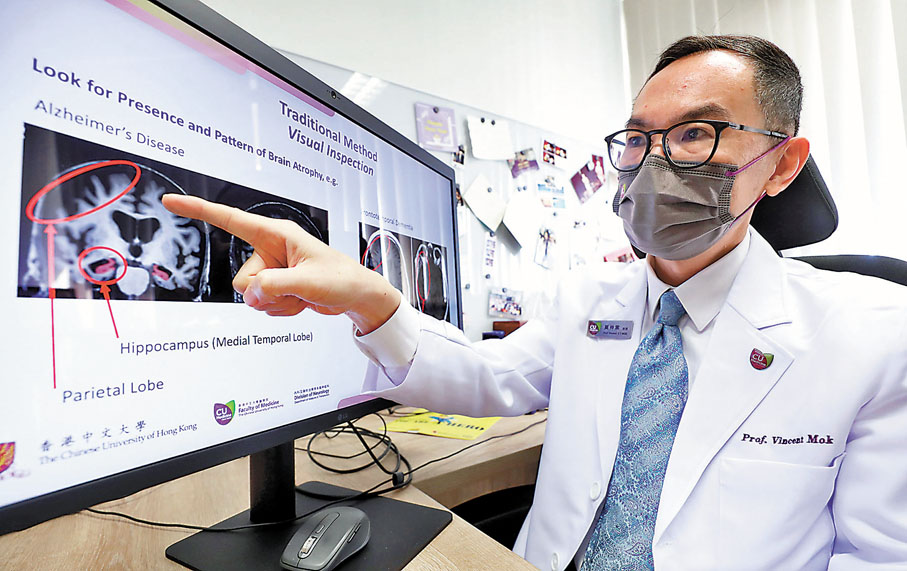
阿茲海默症患者的大腦變化緩慢,哪怕是經驗老到的醫生,也難單憑大腦的磁力共振(MRI)影像辨識早期患者。香港中文大學周佩芳認知障礙預防研究中心主任、醫學院內科及藥物治療學系腦神經科主任(學術事務)莫仲棠及其團隊遂積極研究人工智能結合磁力共振的全新技術,以辨認大腦「容量」的變化及萎縮情況,在10分鐘內得出直觀可靠的「阿茲海默症腦萎縮指數(AD-RAI)」,協助醫生斷症。
為了排除大腦有腫瘤、隱性中風等因素,醫學界普遍會採用磁力共振掃描阿茲海默症患者的大腦,但初期病人的大腦沒有明顯萎縮,因此無法確診。莫仲棠表示,阿茲海默症的其中一項病理特徵為大腦出現β澱粉樣蛋白(Aβ)斑塊,「為了捕捉這些蛋白,要通過正電子放射斷層掃描(PET),但全港只有兩所醫院有相關儀器,每做一次要2萬多元。」若透過腦脊髓液檢查分析,則要透過腰椎穿刺技術偵查異常蛋白,有一定風險。
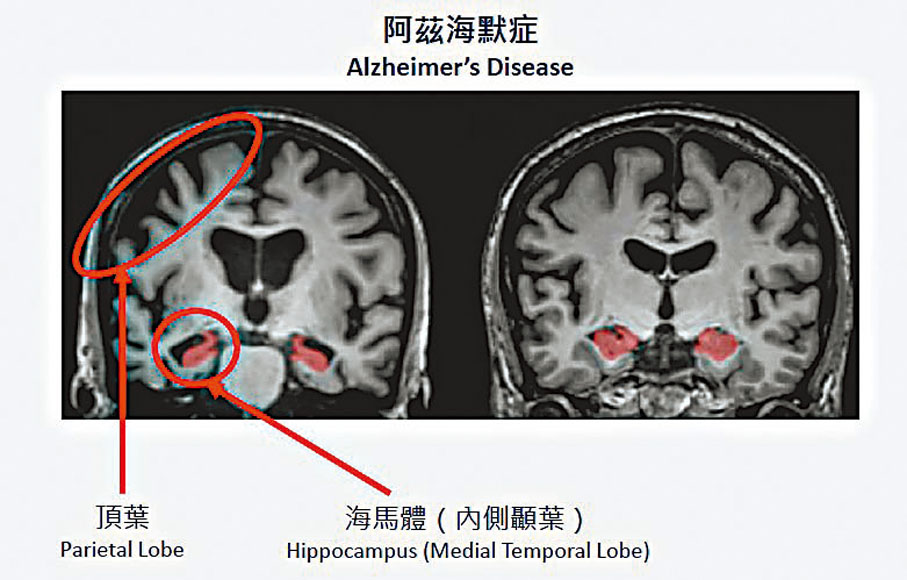
10分鐘比對大腦影像
為克服這個問題,莫仲棠與中大醫學院影像及介入放射學系副教授石林組成的研究團隊,成功研發出全新系統,利用人工智能技術分析磁力共振掃描影像。只需將影像電子化並上載雲端分析系統,系統即會比對數據庫的大腦影像,只需10分鐘即能得出「阿茲海默症腦萎縮指數」,指數範圍為0到1,「分數愈接近1就愈像腦萎縮,0.5或以上就有患上輕度認知障礙的傾向。」
自2019年起,團隊已為逾2,000名長者進行磁力共振分析,其中約600名為阿茲海默症患者、約1,300名認知能力正常的長者、其餘為不同類型的認知障礙症患者。研究顯示,系統在識別輕度阿茲海默症方面,靈敏度高達九成二、識別能力亦高達81%;而整體準確率則為86%。
由於早期阿茲海默症患者的大腦萎縮情況不明顯,人工智能系統可以將大腦體積量化,準確至0.01ml,有助醫生了解患者大腦的細微變化。
此外,不同認知障礙症的大腦萎縮部位不一,系統亦可精準偵測萎縮情況及規律,及早判斷患者所屬類型,包括路易氏體認知障礙症、額顳葉認知障礙症等。
莫仲棠期望新技術能提前一兩年找出輕度患者,而新技術應用範圍廣泛,「幾乎是所有醫院,只要能做到磁力共振的地方就能應用新技術」,而中大醫院、坊間部分MRI中心現已採用有關技術,團隊會持續收集更多用家數據,以提高準繩度。

城大追蹤葡萄糖遊腦速度縮診斷期
阿茲海默症一般被視為「老人病」,但該病有年輕化趨勢,最年輕的案例甚至只有23歲。香港城市大學的團隊研發出嶄新的磁力共振成像方式,透過測量葡萄糖進出大腦的速度,以判斷腦淋巴系統有否阻塞,有望將診斷期限提前至少10年,讓病患尚未出現任何病徵前就可採取介入治療。
阿茲海默症病者大腦中的β澱粉樣蛋白(Aβ)斑塊及 Tau蛋白,讓神經元逐漸壞死,但患者大腦早在10年到20年前已經開始變化,但過程緩慢,愈早斷症愈有利治療。城大生物醫學工程學系副教授、香港心腦血管健康工程研究中心副總監陳葦恩表示,科學界對阿茲海默症的研究有一百多年,「直到2012年,科學界才發現新的腦系統—腦淋巴系統(glymphatic system)」,其中腦脊髓液(CSF)會通過星狀細胞進出腦組織,帶走腦組織中的蛋白質廢物,「若『清除率』較慢,那麼β澱粉樣蛋白容易形成斑塊;腦細胞沒有良好的生長環境,自然就會死亡。」
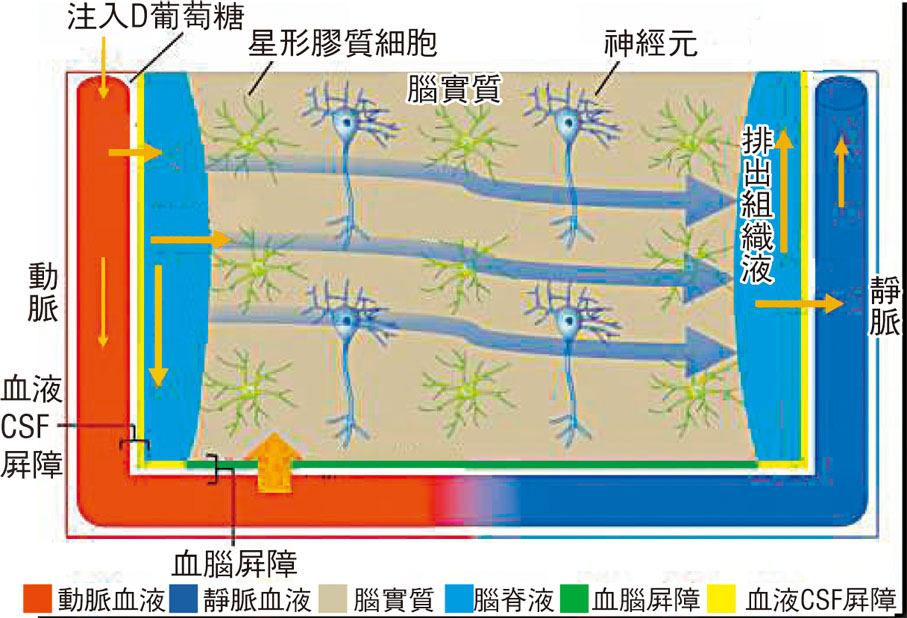
葡萄糖作為大腦的主要能源,測量它在大腦的蹤跡,即可了解「清除」過程有否受到阻礙,故陳葦恩團隊研發的「動態葡萄糖增強磁力共振分子成像」(DGE-MRI),原理是來自動脈的葡萄糖通過血管周邊的葡萄糖運轉蛋白進入腦實質,通過「血液腦脊液屏障」及「血腦屏障」後,大部分腦脊液會循環至腦實質,最後排出組織液。新型DGE-MRI能同時檢測腦實質、脊髓液的圖像,還能提供血腦屏障通透性訊息,測量葡萄糖的攝取及清除過程,意味着在β澱粉樣蛋白形成前,已經能捕捉大腦變化。
研究人員發現,患病小鼠的葡萄糖清除率比正常小鼠顯著降低,其中六個月大小鼠的清除率低於正常小鼠的三倍,若技術發展成熟,可以提早至少10年找出潛在患者。有關研究已經在科學期刊《科學進展》(Science Advances)上發表。
葡萄糖作「示縱劑」非入侵性
至於傳統診斷阿茲海默症的正電子放射斷層掃描(PET),要注射放射性顯影劑,價格高昂又有入侵性,反觀DGE-MRI無創安全,「而天然葡萄糖是大腦的主要燃料,利用其作為『示縱劑』,可以知道腦部利用葡萄糖的功能及大腦受損情況。」新技術還能針對大腦特定區域提供參數,「通過每年的DGE—MRI檢測,醫生透過不同參數變化,可區分正常老化與病變。」當數據庫增大,病患數據甚至可與同齡人比較,提高診斷準確性。
團隊利用3T磁力共振小動物掃描儀進行實驗,其磁場強度與臨床儀器的強度相等,團隊現時與本港個別醫院進行臨床實驗,期望在3年至5年內能正式推出。