免疫治療是近年新興的癌症療法,不但較傳統化療溫和,對患者的副作用亦較為輕微。然而,常用的樹突細胞免疫療法臨床效果參差,細胞培育過程繁複且成本高昂。香港教育大學(教大)科研團隊近日成功研發新型二氧化矽納米基質生物材料(Nanozigzags, NZs),能有效縮短樹突細胞培育時間,降低成本,並將療效提升近70%。

癌症多年來仍是全球及香港的主要致死疾病,2025年更佔全港因疾病死亡宗數的三成。雖然化療仍屬主要療法,但副作用及復發風險持續困擾患者。近年興起的嵌合抗原受體T細胞治療(Chimeric Antigen Receptor T-cell Therapy, CAR-T)雖結合免疫、細胞與基因技術,但對實體腫瘤效果有限,且有機會引發過度免疫反應,成本亦動輒數百萬港元。
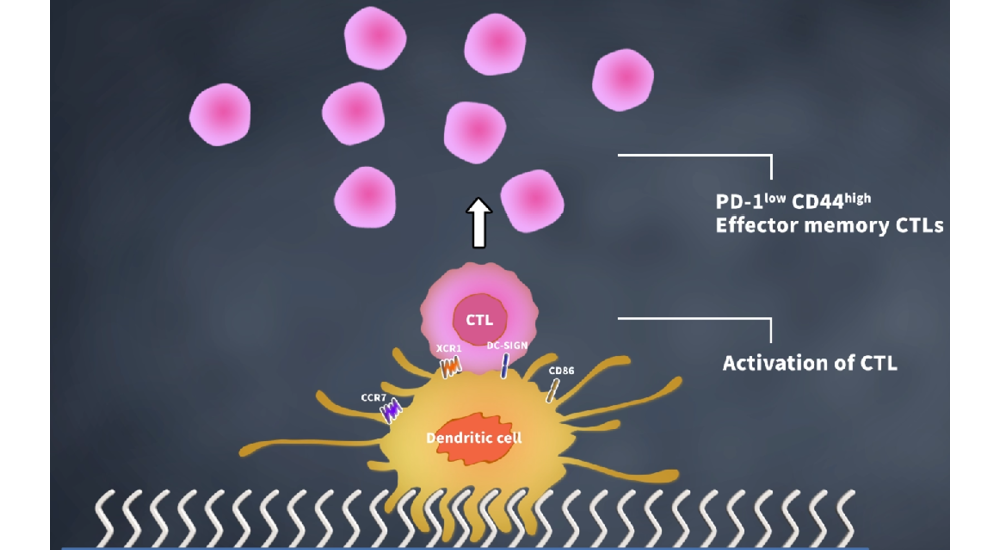
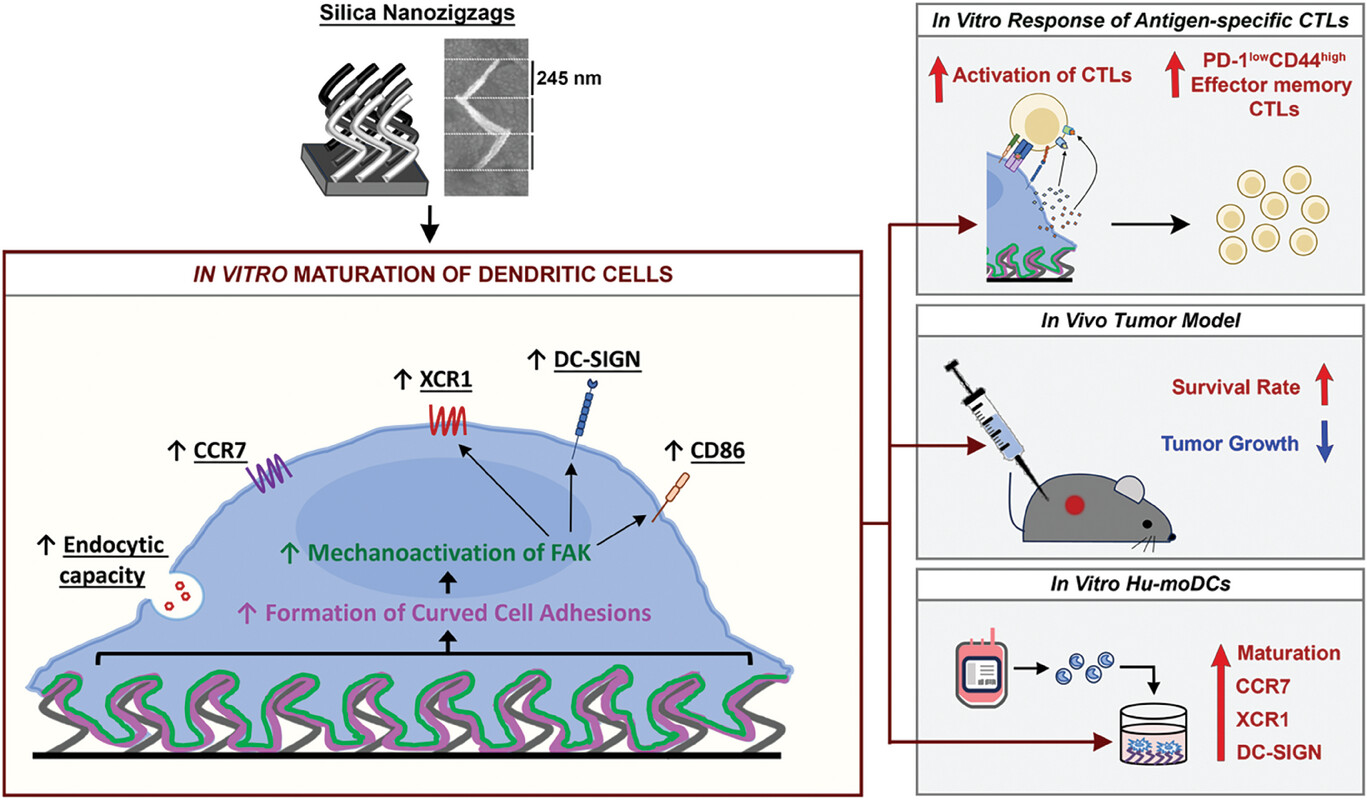
樹突細胞(Dendritic Cell, DC)治療則透過分離病人血液中的單核細胞,在體外與腫瘤抗原共同培養成成熟的樹突細胞,再回輸體內協助免疫系統攻擊癌細胞。雖副作用較少,但療效不穩定,製備過程亦繁瑣。為突破瓶頸,教大科學與環境學系生物與神經科學講座教授兼協理副校長(知識轉移與可持續發展)翁建霖教授領導的團隊,研發出天然無毒且高度生物相容的二氧化矽納米基質。此物料能以安全高效方式促進樹突細胞成熟,顯著增強T細胞對癌細胞的識別與攻擊能力,克服癌細胞「偽裝」問題,提升靶向精確度。動物實驗顯示,新技術能有效抑制腫瘤生長,延長免疫記憶並增強持續性。
研究由教大牽頭,並與香港中文大學、香港浸會大學及暨南大學合作。整個細胞培養過程於體外完成,無需依賴患者自身免疫系統,確保療效穩定,尤其適合化療後免疫力低下的患者。技術設計具備標準化與大規模生產潛力,有助降低成本並加速臨床應用。
翁教授指出,這種新型物料未來更有機會拓展至癌症治療以外的應用。他說﹕「在二氧化矽納米基質環境中,樹突細胞呈現獨特的 Z 形結構,能增加表面接觸面積,更有效傳遞生物物理信號,與傳統培養方式截然不同。我們的研究以生物物理信號取代高風險操作,為 DC 疫苗提供更安全、更易普及的新路徑。未來,我們將進一步探索這種新型樹突細胞在系統性紅斑狼瘡,以及多發性硬化症的潛在應用,期望為免疫調節療法開拓新方向。」
研究團隊計劃與本地及內地的醫院及實驗室合作,加速細胞培養和療效測試,推進臨床研究。