香港文匯報專題組:內地製藥技術不斷提升,惟香港沿用港英時期的西藥註冊制度,令一些內地研發藥物或歐美以外地區研發藥物在港註冊困難重重,導致香港藥物來源十分狹窄,甚至出現被壟斷的情況。香港文匯報將剖析現行制度導致日常藥物及癌症等「救命藥」的樽頸,令病人的藥物選擇少、無藥可醫,今年初患上足底疣的羅先生就深受其害。為治病,他曾向公立醫院求診,卻因疫情預約無期,遂向私家醫生求醫,被建議接受收費7萬元的手術,而醫生更明言未必可以「斷尾」。其後,他得悉內地研發的一款數十元人民幣專利藥膏能治此症,惟藥廠早年申請來港註冊不果,羅先生只得經朋友從內地帶藥來港,服後只花2.5個月即痊癒,「真神奇,幾十蚊搞掂,效果可能好過幾萬蚊的手術,香港唔畀佢註冊係走寶!」
目前,在港註冊的處方或非處方西藥必須獲得最少兩個「認可國家」註冊才能在港出售。該「認可國家」名單包括32個歐美等國家及地區,但未包括內地或亞洲一些新崛起的製藥強國,令香港市面的藥物多為歐美進口,導致選擇少、醫療成本高,一些情況下更令治病市民白走「冤枉路」。
羅先生今年初患上足底疣(又稱跖疣、病毒疣),是一種由人類乳頭瘤病毒(HPV)所引起的疾病。他近日在接受香港文匯報訪問時坦言,自己最初見到其腳趾下方長出貌似繭的東西時,還以為只是「雞眼」,故不以為意,「過了兩個月腳板底突然痛,幾天後發現腳底幾處都痛,個繭帶有水泡,先知唔係雞眼,上網查懷疑係足底疣。」從事戶外工作的他每天要走動和站立數小時,其工作飽受足底疣的困擾,「企住唔郁都痛,行路就完全唔掂。」
他遂預約公立醫院門診,惟當時遭逢新冠肺炎第五波疫情最嚴重的時期,「根本預約唔到期,我就效法網民的經驗,用白醋泡腳、水楊酸去死皮。」然而,這些方法治標不治本,更延誤治療,導致足底疣擴散,由最初單腳受感染惡化至雙腳都有患處,最嚴重時多達數十個患處,「陣時已經痛到無法企,行路就好似踩鐵釘上面,但工作時需要走動,試過忍痛行一個鐘左右雙腳就麻木。」
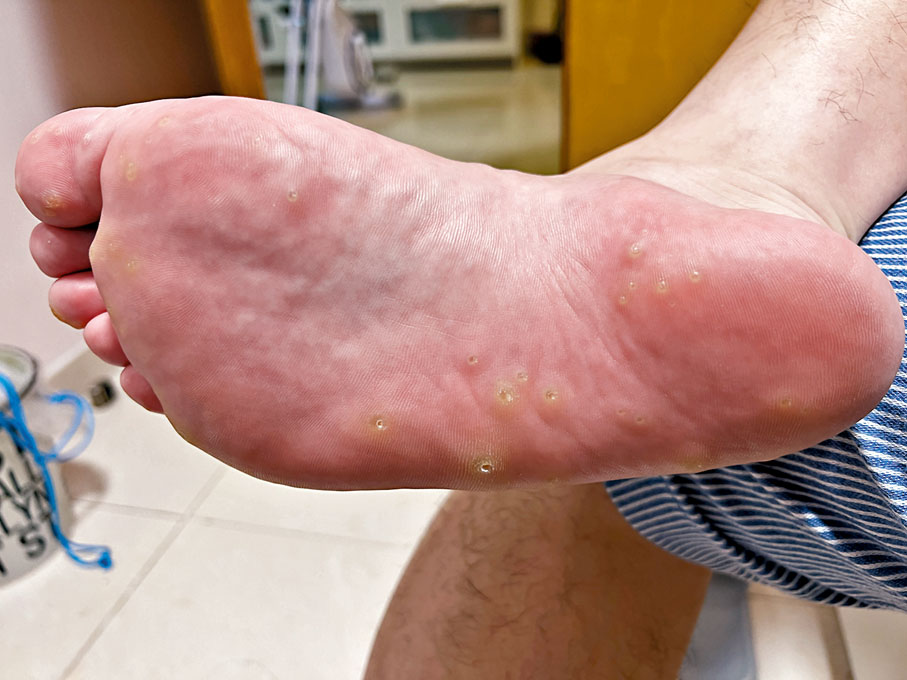
難耐每天受腳痛折磨,向公立醫院求醫不果的羅先生唯有向一名私家皮膚科醫生求醫,對方一看就診斷為足底疣,表示目前香港常用手術方法治療,包括液氮冷凍、激光及電灼刮除手術,「醫生話我腳底疣大大小小接近50粒,數量太多,冷凍同激光都不合適,唯有用電灼。」
醫生明言手術未必可「斷尾」
然而,電灼手術價格之高昂令羅先生卻步:5次手術費共花7萬多元,每次相隔半個月,金錢及時間成本不菲,卻不一定能根治,「醫生講明手術完成後,仍有兩成機會復發。唔係畀唔起,而係覺得唔值。」
足底疣是常見的皮膚病,但由於香港皮膚科醫療資源緊缺,通常只能依靠手術治療或普通藥物緩解不適,而在內地這樣的常見皮膚病病人眾多,因此有豐富的治療經驗,內地更研製了一款專利外用藥物。羅先生在內地親戚的幫助下,諮詢了內地一名公立醫院皮膚科醫生,經推薦該藥後由親戚帶來香港。這款不起眼的藥膏在內地售價僅數十元人民幣一支,但羅先生使用近兩個月後,足底的疣已完全脫落,痊癒至今半年都未有復發。
有關藥物為香港李氏大藥廠在內地的子公司兆科藥業(合肥)自主研發的產品,除可治療人類乳頭瘤病毒等引起的皮膚疾病外,對新冠病毒也有預防作用。2020年,該藥更被安徽省和國家工信部列為新冠疫情下的緊缺戰略物資。早年,該公司嘗試申請該藥在港註冊,但現行制度充滿保護主義,這些內地藥難獲歐美等「認可國家」註冊,故無緣在港合法發售,造福更多病人。
藥廠批港審批制度落後
李氏大藥廠創辦人李小羿早前向傳媒表示,香港新藥審批制度落後、態度保守。在這種制度下,香港對內地研發的藥物有所保留,但歐美藥廠又不會專門研發適用於亞洲市場的新藥(如鼻咽癌藥物),令香港出現「兩頭不到岸」的尷尬情況。
西藥在港註冊兩途徑
途徑一:在任何兩個「認可國家」註冊
「認可國家」包括:澳洲、日本、美國、英國、保加利亞、塞浦路斯、愛沙尼亞、拉脫維亞、立陶宛、馬耳他、斯洛伐克、斯洛文尼亞等32個國家
途徑二(上月新增):巴西、中國內地、韓國或新加坡註冊的藥物,再加一個「認可國家」註冊
話你知|涉保護主義 四地藥難獲「認可國家」註冊
香港的西藥註冊制度沿襲自港英時期。當時,由於香港並無人力物力去自行審批每款藥物,故要求在港發售的西藥必須獲兩個或以上的「認可國家」註冊,而「認可國家」包括32個國家及地區,內地暫不在名單內,但諷刺的是,名單上不少歐洲小國,其醫療水平落後於內地。香港衞生署雖於上月開闢新的註冊途徑,讓內地、巴西、新加坡和韓國四個地區研發的西藥,只要獲任何一個「認可國家」註冊,就能在港發售,但藥劑業界指出,全球製藥業充滿保護主義,四地藥物難獲「認可國家」註冊,最終受損的是香港病人。
香港醫院藥劑師學會會長崔俊明向香港文匯報解釋,在新措施下,藥物有兩種途徑獲取香港註冊的「入場券」,「要麼在32個『認可國家』中獲最少兩國的註冊;要麼屬內地、巴西、新加坡或韓國四地區的註冊藥物,並最少在一個『認可國家』註冊。」
新途徑看似放寬了,但崔俊明認為實際意義有限,「32個『認可國家』,以美國FDA(美國食品藥物管理局)為龍頭。基於保護主義、地緣政治等原因,內地藥品要在美國等『認可國家』註冊幾乎不可能。換言之,很難來港註冊。」
藥劑界醫學界:制度不合時宜
藥劑界和醫學界均認為這制度不合時宜,他說:「現在香港已回歸祖國,內地製藥技術又提升不少,這個制度有改善空間。」
臨床腫瘤科專科醫生區兆基解釋,香港當年在制定「認可國家」名單時,主要考慮有關國家是否已加入3個國際機構,包括ICH(國際醫藥法規協和會)、SRAs(世衞參與制度的嚴格監管機構)和PIC/S(國際醫藥品稽查協約組織),而中國國家藥監局已於2017年加入ICH,翌年當選為ICH管委會成員,但仍未加入SRAs和PIC/S。
他指出,ICH除了參考成員國的藥物質量、安全、交叉科學外,在有效性方面尤其重視臨床研究,較全面評估一個國家的藥物質量;SRAs是由世衞秘書處和全球抗擊愛滋病、結核病和瘧疾基金制定,用於指導藥品採購決策;PIC/S旨在建立藥品製造的良好生產規範(GMP)。相比之下,ICH與藥物的關係性較大,「既然國家藥監局已加入ICH並成為管委會成員,足以證明內地藥物的製造及臨床試驗具有相當高的標準。」
身為醫生,區兆基會較看重ICH成員國的名單,而是否屬SRAs和PIC/S成員國純粹「錦上添花」。因此,香港沒有必要參考其他小國的標準,並建議衞生署優化該名單、重設審批標準,設立以ICH標準為主的新「認可國家」名單。
特寫|內地藥難來港 港人無奈捱貴藥
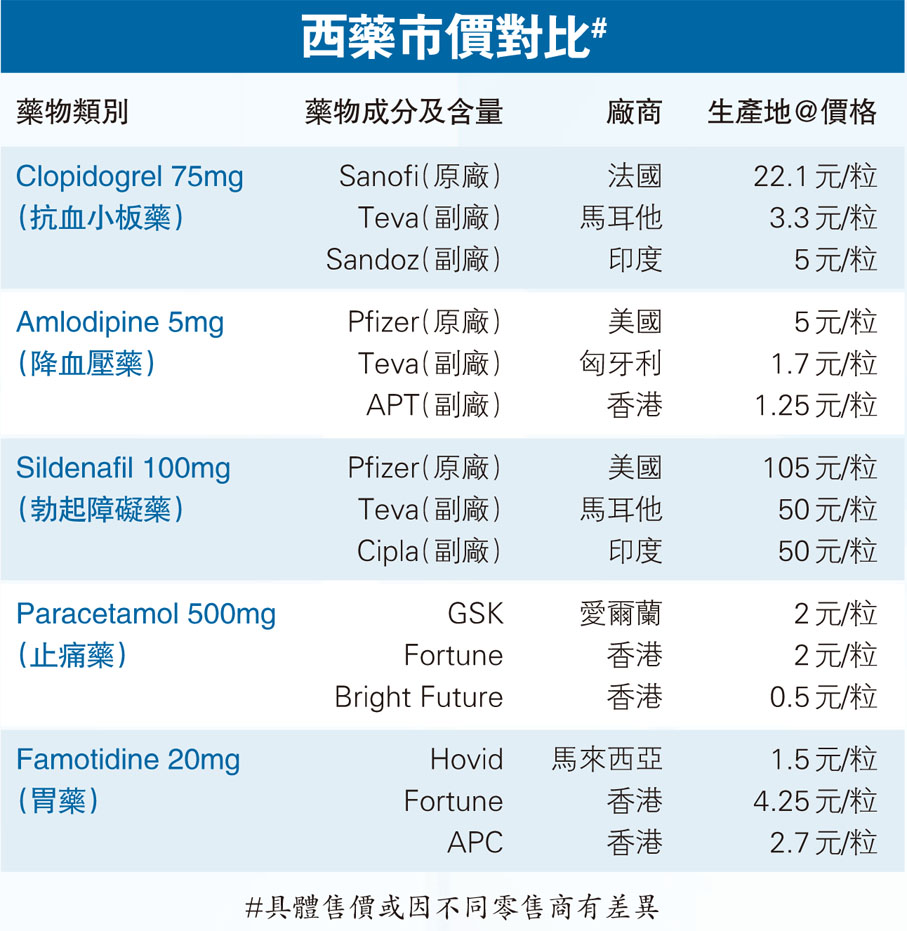
香港文匯報記者日前到港九各持牌藥房和個人護理連鎖店,發現無論是處方或非處方的西藥,都不見內地藥物的身影,主要以歐美和日本藥為主。有藥房老闆表示,內地藥難獲註冊,港人只能捱貴藥,特別是處方藥通常是正廠貴、副廠平,不同藥廠生產的同款藥差價最高或達7倍至10倍。

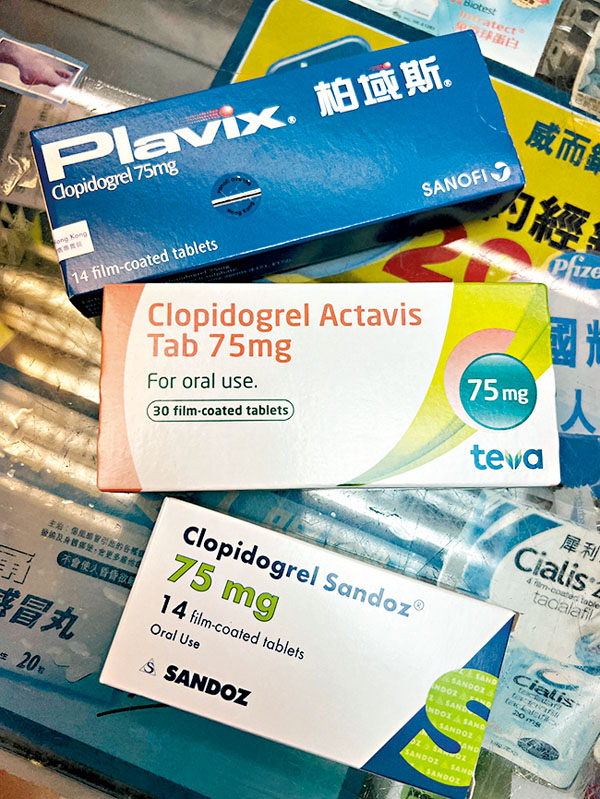
該業內人士解釋,這些藥一般是原廠研發,專利期間貴價發售,專利期限過後,其他藥廠都能根據相關主要成分制定配方生產,獲32個「認可國家」中兩國註冊就可申請進口香港,藥價一般較低。儘管原廠與副廠差價大,大多數顧客仍選擇原廠,「無論效果究竟是不是一樣,顧客都會有心理作用,覺得原廠、大牌子好,有信心。小部分選擇副廠的用家亦並非完全考慮價格,而是因為醫生推介。」
非處方的藥物就可見不少香港藥廠的身影,如傷風感冒藥、止痛藥、腸胃藥、皮膚藥膏等。業內人士指出,這些藥部分歷史悠久,在未有「認可國家」註冊制度前已在港發售,故可豁免在該制度下註冊。
(來源:香港文匯報A03:要聞 2022/12/15)