國產甲流疫苗進臨床驗證
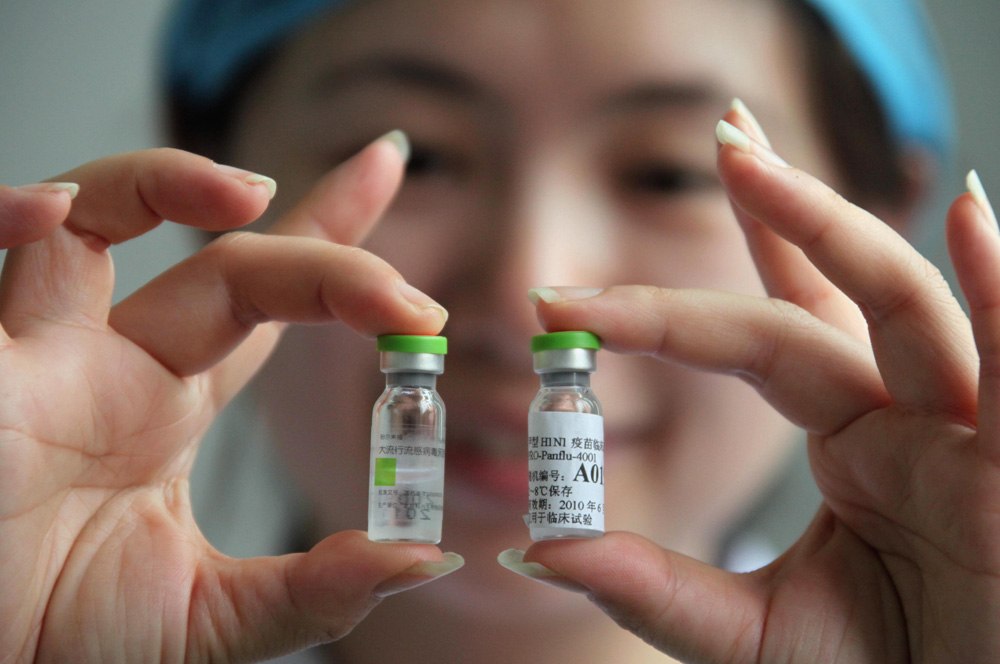
圖:醫務工作者22日展示甲型H1N1流感疫苗(新華社)
記者22日從河南新鄉華蘭生物疫苗有限公司(下稱:「華蘭生物」)獲悉,由該公司生產的內地首批甲型H1N1流感疫苗在完成生物、生化實驗後,當天上午在江蘇泰州正式開展臨床驗證研究,如果一切順利的話,可望在9月份後投入生產。
【本報記者楚長城、于建國,
通訊員呂成玉新鄉二十二日電】
今次臨床驗證研究工作由中國醫藥城牽頭,江蘇省泰州市疾控中心具體組織實施,採用華蘭生物生產的甲型H1N1流感疫苗,並在泰州招募2000多名志願者參與,分批於本月22日、24日和25日接種。
方案已通過專家論證
據悉,接種分為五個年齡組,免疫程序為0天、21天各接種1次,於0天、21天、35天、42天採血檢驗測定抗體滴度,並建立志願者「一人一檔」,一直進行跟蹤回訪六個月。甲型H1N1流感疫苗臨床驗證研究工作,旨在通過臨床驗證研究進一步確認該疫苗的類型、劑量和免疫程序,是大規模生產流感疫苗的重要前提基礎工作。
華蘭生物具有每月1500萬瓶、全年最大1.6億劑單型流感疫苗的生產能力。6月3日,該公司獲得可用於甲型H1N1流感疫苗生產的毒株後,啟動疫苗的生產研發;6月22日,首批用於工藝研究的甲流疫苗問世;7月3日,用於人體臨床試驗的產品送交中國藥品生物製品檢定所;7月5日,臨床試驗方案通過國家CDC組織的專家論證。
據媒體此前報道稱,在臨床試驗順利的情況下,有望在9月份獲得生產文號,之後即可批量生產。
華蘭生物深圳曾停牌
華蘭生物工程股份有限公司(證券代碼:002007)今天午間公告稱,集團子公司(河南新鄉華蘭生物疫苗有限公司)研製的甲型H1N1流感疫苗正式進入臨床驗證階段,鑑於上述臨床驗證結果及生產甲型H1N1流感疫苗尚需國家食品藥品監督管理局的正式批准等諸多不確定性因素,有關疫苗的上市時間仍存在不確定性。
華蘭生物預計,今次臨床觀察大約需要40多天時間,將驗證疫苗的安全性、有效性,最終確定疫苗的免疫程序和免疫劑量。
深圳證券交易所今天早間發布公告稱,華蘭生物披露今次臨床驗證研究工作重大事項進展情況,申請公司股票於今天開市時起停牌。而下午1時起,華蘭生物公司股票復牌。
加速形成疫苗產業鏈
今次臨床驗證研究工作是中國醫藥城疫苗工程中心組建以來實施的首次臨床研究。該中心是一個集疫苗研發、臨床研究、檢測為一體的綜合性服務機構,承接全國大量的疫苗臨床研究工作,同時為區內疫苗產業基地落戶企業提供研發服務和技術指導。
中國醫藥城規劃建設以來,致力於打造內地規模最大、產業鏈最完善的疫苗產業集群,目前已集聚了國內外12家疫苗研發、生產及銷售企業,上下游垂直整合的疫苗產業鏈正在加速形成。
