【科學講堂】化合物令血液速凝固 啟發生物醫學
當我們受傷、流血時,慶幸血液會自行凝結成塊,堵塞傷口,避免持續失血。然而,這些血塊並非十分堅固,劇烈動作或擠壓便可能使其破裂,導致傷口再次暴露。本文將與讀者分享一項近期發表於國際頂尖學術期刊《Nature》的研究成果,該研究提供了一種全新方法,能使血液在數秒內凝結成更為扎實的血塊,從而為傷口帶來更有效的保護,並顯著促進組織再生。
體內的止血現象,是一連串複雜的生化反應,當傷口出現時,身體會產生血纖維蛋白(fibrin),並編織成一張網狀結構。這張由血纖維蛋白構成的網絡能將附近的紅血球連接起來,進而形成血塊。
然而,此凝血過程相對緩慢,通常需要數分鐘,且形成的血塊亦不夠堅固,因紅血球雖然佔據血塊近一半的體積,卻幾乎無法提供硬度,而真正承擔結構支撐作用的纖維蛋白網僅佔不足1%。因此,天然血凝塊在生理血壓下極易破裂或脫落,遭遇較大機械應力時往往失效,嚴重限制了其止血效果。
血凝塊強度升13倍
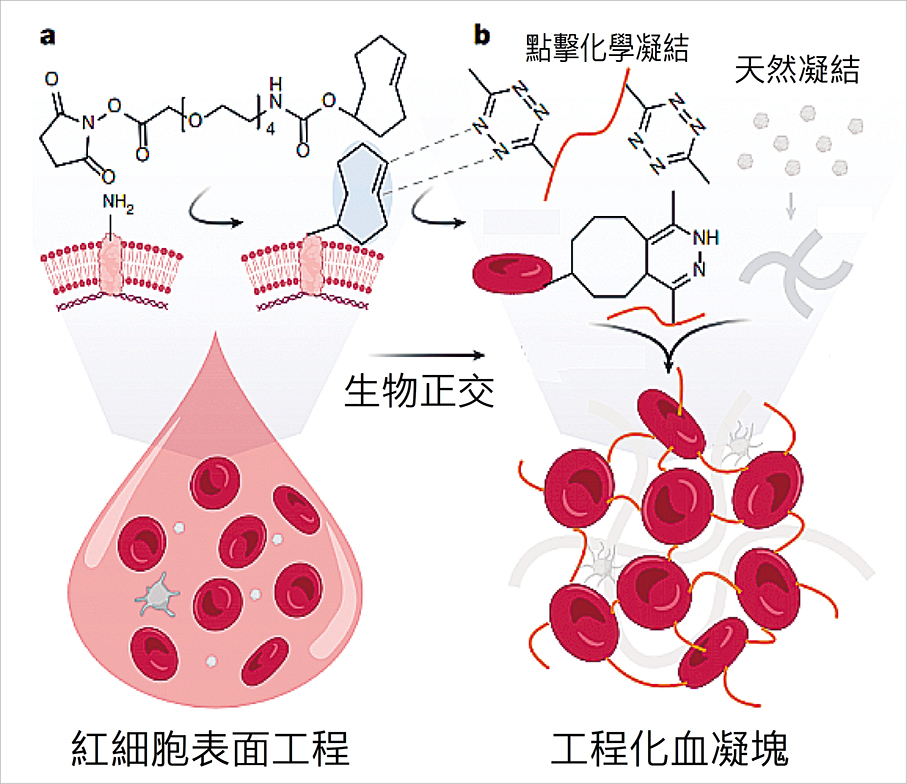
研究人員在紅血球表面引入有機化合物反式環辛烯(Trans-Cyclooctene),然後將這些修飾後的紅血球與含有四嗪(Tetrazine)官能團的聚合物混合(如圖)。
反式環辛烯與四嗪之間會發生超快速的生物正交點擊化學(Click Clotting)反應,從而在數秒內將紅血球通過共價鍵連接起來,形成一種名為「細胞凝膠」(cytogel)的連續細胞網絡。這個細胞凝膠進一步與天然凝血過程中形成的纖維蛋白網絡交織,共同構成了工程化血凝塊(Engineered Blood Clots, EBC)。在此體系中,紅血球不再是被動的填充物,而是直接參與承載外力,從根本上改變了血凝塊的結構屬性。
這種經過改良的凝血機制在多項性能指標上取得了亮眼的成績。首先,反式環辛烯與四嗪均不會參與其他化學反應,具有優異的生物正交性,因此不會影響血液中原有的生化過程。其次,此改良方法顯著增強了血塊的韌性和黏附力:與人體天然形成的血塊相比,工程化血凝塊的斷裂韌性(fracture toughness)提升了13倍,與組織的黏附能量(adhesion energy)也提升了4倍。
這一卓越的韌性提升,源於一個全新的力學機制。研究發現,細胞凝膠的韌性提升並不依賴於增加聚合物含量,而是來自細胞本身。當外力作用時,工程化血凝塊中那些被共價交聯、主動承力的紅血球會依次發生物理破裂,從而來吸收並耗散大量能量。這種類似「犧牲結構」的機制,有效抑制了裂紋擴展,使工程化血凝塊在受到衝擊或拉伸時不易發生災難性斷裂。
在實際應用層面,此改良凝血機制也展現了非凡的潛力。在老鼠的肝臟傷口模型中,工程化血凝塊可在5秒內形成血塊,顯著減少血液流失。更令人矚目的是,在大鼠肝臟大面積切除的嚴重損傷活體實驗中,該血凝塊能夠助力肝臟完全癒合、恢復至正常大小,且未留下明顯疤痕。
相比臨床使用的產品,工程化血凝塊還將術後肝臟與周圍組織的黏連率從83% 大幅降至17%。
此外,該技術還展現出優異的生物相容性和極低的免疫反應,無論是使用自體血液(約20分鐘製備),還是同種異體捐贈的配型血液(約10分鐘製備),均能有效快速止血。研究團隊更發現,該機制的「點擊凝血」思路具有通用性,可應用於其他類型的細胞,包括構成結締組織的成纖維細胞、脂肪來源幹細胞,甚至單細胞藻類,顯示其在未來生物醫學領域具有廣泛的應用潛力。
然而,要進一步將此改良凝血機制應用於實際醫療環境,仍存在一些問題需要解決。例如,該機制需要使用特定的試劑與處理步驟,因此未必能輕易融入高壓力、高速度的醫療場景。此外,降低成本以及在大型動物身上進行測試,也是後續必須進行的步驟。
除了將紅血球連接起來形成血塊,此技術還可能有其他令人興奮的應用:例如,將細胞連接以協助器官再生,甚至製造出新器官;或者將免疫細胞聯結起來,形成對抗癌症的防線。這項研究將血凝塊從一種自然產物,轉變為一個「可設計的材料體系」,為創傷急救、外科手術和再生醫學提供了全新的策略和思路。
●杜子航 教育工作者
早年學習理工科目,一直致力推動科學教育與科普工作,近年開始關注電腦發展對社會的影響。
