【城市TechTalk】果蠅疾病模型分析 突破肌萎治療瓶頸

談到嚴重疾病,大眾一般較為熟悉癌症、心臟病等,罕見病往往被忽視。由於相關研究相對較少,因而令這類疾病的治療方案較傳統及局限。為了讓罕見病患者獲得更佳治療方案,筆者與團隊專注於罕見疾病研究。今期《青談科研》為大家介紹筆者團隊的最新研究發現,揭示第一型肌肉強直症(DM1)致病基因如何損害神經系統,期望為患者帶來新的針對性治療方案。
DM1是一種肌肉萎縮症,全球患者不足一萬名,屬罕見疾病。患者的肌肉會逐漸變得無力、萎縮及僵硬,導致行走困難,同時會有心律不整、呼吸困難及認知障礙等情況出現。
2006年至2016年間本港醫院分析91名DM1患者的腦組織數據,結果顯示患者染色體上的肌強直性營養不良蛋白激酶(DMPK)基因,出現CTG三核苷酸序列異常重複,次數高達數百至數千次,遠高於正常人重複不多於37次的頻率。不過,過往針對DM1的研究大多集中於肌肉病變,鮮有深入探討其引發的神經系統問題,如神經突觸功能失調、神經元流失等關鍵機制破壞。
神經系統影響未受重視
舉例說,人體肌肉就如一個燈泡,神經則是一個燈掣。如果燈泡不能發光(即肌肉不能正常活動,出現DM1症狀),可能是燈泡(肌肉)或是燈掣(神經)損壞,亦有可能是兩者同時受損。過往研究大多集中於肌肉受損這一部分,至於DM1對神經系統的影響,長期以來未受到與肌肉病變的同等重視,故此筆者團隊希望可以提升對這方面的關注。
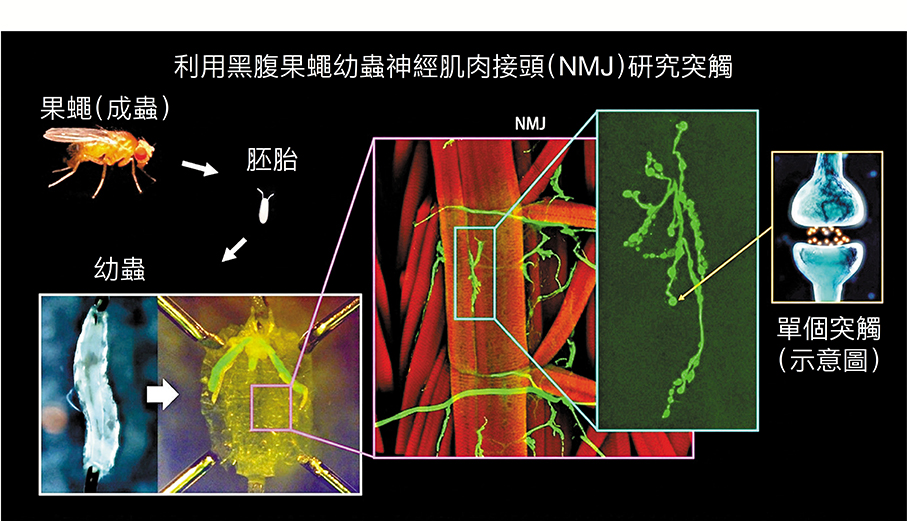
今次研究通過轉基因DM1果蠅疾病模型,觀察及分析其神經突觸的變化,結果發現:果蠅體內的CTG三核苷酸序列異常重複,會導致其FasII蛋白過度表現,這正是引神經突觸流失的關鍵因素。果蠅的FasII蛋白,功能上相等於哺乳類動物,包括人類細胞的黏附分子NCAM1,研究團隊其後在小鼠DM1模型實驗中進一步證實,NCAM1同樣表現異常。這種異常導致他們的NCAM1表現失調,引致RNA毒性致病機制,最終造成神經突觸流失及肌肉壞死。
再以燈炮與燈掣做比喻:NCAM1 就像連接燈掣及燈泡的電線,一旦出現異常,燈掣及燈泡均會故障,對應到人的身體即是肌肉及神經同時受損,進而出現DM1的症狀。研究亦發現,動物模型若僅單一出現肌肉或神經受損,症狀只屬輕微。
這就說明,除了肌肉病變外,神經系統損傷同為DM1致病元兇。
今次研究為治療DM1帶來新的治療方向。過往治療方案只集中於減緩肌肉退化及流失,缺乏針對神經系統的治療策略,只能「頭痛醫頭,腳痛醫腳」,未能從根源改善。
這個研究則明確發現DM1發病與神經突觸病變有關,證實調控果蠅體內FasII蛋白表現,可有效修復突觸缺陷,為臨床治療找出了可行的治療靶點。未來開發DM1治療方向時,可以循着同時保護患者肌肉以及神經元的藥物新方向推進,為開發針對病因的療法邁出重要一步。
下一階段,團隊將致力研發同時針對修復肌肉及神經元的藥物,包括小分子藥物、生物製劑或疫苗等,期望為DM1患者治療帶來更具根治性的治療曙光。
●圖、文:香港青年科學院提供
授課人:陳浩然教授
香港青年科學院創院院士
香港中文大學生命科學學院
